近日,南京农业大学动物科技学院孙少琛教授实验室在发育生物学权威杂志《Development》(5 year IF=6.134)上在线发表题为“Rab23/Kif17 regulate meiotic progression in oocytes by modulating tubulin acetylation and actin dynamics”的研究论文,深入研究了卵母细胞成熟过程中的细胞骨架动态调节机制。孙少琛教授为通讯作者,博士研究生王洪晖为第一作者。该研究得到了国家重点研发项目、国家自然科学基金、中央高校基本科研业务费等项目的支持。
对于哺乳动物而言,新生命个体的发育起源于由来自父方的精子和来自母方的卵子所结合而成的受精卵。虽然这两种生殖细胞都携带着未来个体一半的遗传信息,但是在体积上二者存在着明显的差距。在进化过程中,卵母细胞成为了具有较大胞质体积的一方,这也为后面的受精以及初期的胚胎发育提供了丰厚的物质基础。因此,高质量的卵子对于后代的发育起着至关重要的作用。然而,调控卵子成熟和质量的机制非常复杂,仍然需要深入研究。
细胞骨架动态参与到了卵母细胞成熟的诸多过程,比如纺锤体组装、迁移以及极体的排出等。而囊泡运输蛋白和驱动蛋白对于细胞的信号传导和物质转运起到重要的传递作用。该研究发现,囊泡运输蛋白Rab23能够调控驱动蛋白家族成员Kif17沿着细胞骨架的运动行为,从而影响Kif17所携带的特定物质到达目的地去发挥作用。通过构建点突变质粒,经体外转录后的mRNA显微注射,该研究发现结合GTP的Rab23活性形式能够促进Kif17对于微丝调控因子RhoA-ROCK-LIMK-cofilin通路和微管翻译后修饰相关因子αTAT和Sirt2的转运,从而调控二者的装配与稳定性。但是,敲低Rab23或者过表达结合GDP的Rab23非活性形式则会影响以上因子的转运,并造成卵子成熟率下降、质量降低等问题。本研究发现了调控卵子成熟的一条新通路,将囊泡运输蛋白与驱动蛋白家族成员统一于调控细胞骨架动态的复杂网络之中,加深了人们对于卵子成熟与质量调控的认识,为揭示卵子功能异常、质量低下提供了理论支持。
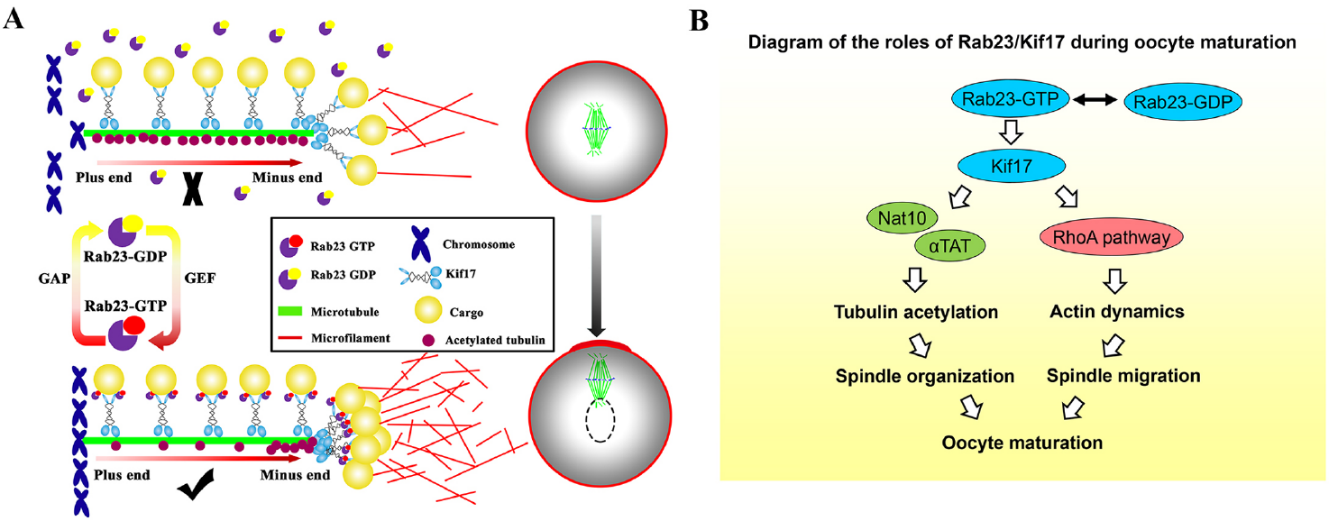
(Rab23通过调控Kif17对于微丝及微管组装相关因子的转运而调控小鼠卵母细胞的成熟进程)
在线连接:http://dev.biologists.org/content/146/3/dev171280